光学纯的吲哚和吡咯并环结构广泛存在于各种天然产物和药物分子中。通过使用分子内的不对称烷基化反应来构建此类并环结构是最为有效和直接的方法。然而使用这种策略来构建吲哚和吡咯并环的成功例子并不多。虽然很多分子内不对称烷基化反应被认为是经历了螺环中间体,然后再迁移为并环产物的历程,但是文献中并没有对这样的反应进行机理层面上的深入研究。通常情况下,如果忽视了反应中这种螺环中间体的形成,往往会造成对反应机理的错误理解,甚至导致烷基化反应产物的结构的误判。
最近几年来,金属室的游书力研究员课题组一直致力于过渡金属催化的不对称烯丙基去芳构化反应研究(Angew. Chem. Int. Ed. 2012, 51, 12662-12686.)。最近,他们发现通过使用金属铱催化的分子内不对称烯丙基去芳构化/迁移的串联反应可以实现吲哚和吡咯并环的构建。通过使用他们小组自己设计合成的新型N-芳基亚磷酰胺配体(L1)和商业可得的金属铱前体可以以高达99% ee的对映选择性得到目标产物。在对该反应的机理进行深入研究后,他们发现该反应首先生成了去芳构化的螺环中间体I,然后I发生了进一步现场的亚甲氨基迁移,得到了新型的吲哚并环结构。该反应模式实现了吲哚底物中的C-3位取代基现场迁移到了C-2位(吡咯底物则是实现了原料中的C-2位取代基迁移到了C-3位),并且在该迁移过程中,反应仍以高的对映选择性得到目标产物。这种新型反应模式的发现不但更正了以前文献报道的关于吲哚分子内烷基化产物结构的误判(J. Am. Chem. Soc. 2006, 128, 1424),而且提供了一条合成手性吲哚和吡咯并环结构的新思路。这部分工作以通讯的形式在《美国化学会志》杂志发表(J. Am. Chem. Soc. 2013, 135, 8169-8172.)。
该项工作获得国家自然科学基金委,科技部、中科院和上海市科委的资助。
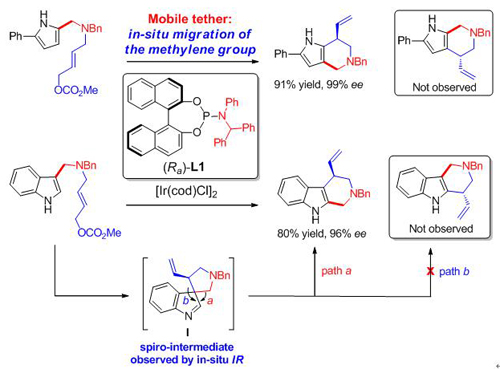
金属铱催化的吲哚和吡咯不对称烯丙基去芳构化/迁移串联反应
